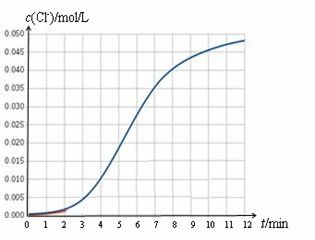

化学反应速率是指化学反应在单位时间内所达到的反应程度,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。

反应速率是指反应体系在某一浓度或压力下的瞬时反应速率或平均反应速率,单位通常为摩尔/平方米·秒(mol/m2·s)或摩尔/立方米·秒(mol/m3·s)。

反应速率的单位通常为摩尔/平方米·秒(mol/m2·s)或摩尔/立方米·秒(mol/m3·s),也可以用其他单位来表示,如摩尔/升·分钟(mol/L·mi)或摩尔/升·小时(mol/L·h)等。

1. 温度影响:一般来说,温度升高,反应速率也会提高,因为高温可以使分子间的碰撞更加激烈,从而提高了反应速率。
2. 浓度影响:一般来说,反应物的浓度越高,反应速率也会提高,因为高浓度的分子碰撞机率增加,从而提高了反应速率。
3. 压力影响:对于气体反应来说,压力越大,反应速率也会提高,因为压力增加可以使气体分子的浓度提高,从而提高反应速率。
4. 催化剂影响:催化剂可以降低化学反应的活化能,从而提高反应速率。不同的催化剂对不同的化学反应有不同的影响。

1. 实验目的:通过实验了解影响化学反应速率的因素,掌握化学反应速率的测定方法。
2. 实验原理:通过改变实验条件,如温度、浓度、压力等,观察化学反应速率的改变,从而了解这些因素对化学反应速率的影响。
3. 实验步骤:(1)准备实验器材和试剂,如试管、滴定管、烧杯、温度计、压力计、催化剂等。(2)按照实验要求将实验试剂加入试管中,并设置好实验条件,如温度、浓度、压力等。(3)开始计时,并观察记录反应速率的变化情况。(4)在实验过程中可以改变实验条件,如温度、浓度、压力等,观察反应速率的改变情况。(5)在实验结束后对实验结果进行分析和讨论。
4. 实验结果分析与讨论:根据实验结果分析不同因素对化学反应速率的影响,并讨论实验结果是否符合预期。同时也可以探讨不同因素对化学反应速率的影响机制。
5. 技能应用与拓展:将所学的化学反应速率演示技能应用于实际教学中,帮助学生更好地理解和掌握化学反应速率的概念和影响因素。同时也可以进一步拓展该技能的应用范围,如应用于工业生产、环境保护等领域。